Urso
Le Informazioni Presenti Sul Sito Non Costituiscono Consulenza Medica. Non Vendiamo Nulla. L'Accuratezza Della Traduzione Non È Garantita. Disclaimer
Riepilogo della droga
Cos'è Urso?
Urso (ursodiolo) è un Anche acido usato per trattare piccoli calcoli biliari nelle persone che non possono avere cistifellea chirurgia e prevenire calcoli biliari nei pazienti in sovrappeso sottoposti a rapida perdita di peso. Urso viene anche usato per trattare la cirrosi biliare primaria (PBC). Urso è disponibile in generico modulo.
Quali sono gli effetti collaterali di Urso?
Urso
Effetti collaterali Lipitor Atorvastatina 40 mg
- nausea
- Dolori di stomaco superiore
- prurito
- sensazione stanca
- perdita di appetito
- urina scura
- sgabelli color argilla
- ingiallimento della pelle o degli occhi
- Spolume improvvisa o mal di sensazione
- febbre
- brividi
- mal di gola
- piaghe da bocca
- piaghe della pelle e
- difficoltà a deglutire
Ottieni subito assistenza medica se hai uno qualsiasi dei sintomi sopra elencati.
Gli effetti collaterali comuni di urso includono:
- Sconturoso o dolore allo stomaco
- nausea
- diarrea
- stipsi
- vertigini
- sensazione stanca
- mal di schiena
- perdita di capelli
- mal di testa
- febbre
- brividi
- Dolori del corpo
- sintomi dell'influenza
- che cola o naso chiuso
- tosse o
- sintomi a freddo.
Dì al tuo medico se hai improbabili ma gravi effetti collaterali di Urso:
- debolezza
- gonfiore delle caviglie o dei piedi
- Sete o minzione aumentata
- segni di infezione (ad es. Febbre persistente mal di gola) o
- Sanguinamento facile o lividi.
Cerca cure mediche o chiama il 911 contemporaneamente se hai i seguenti gravi effetti collaterali:
- Sintomi di occhiali gravi come la perdita di visione improvvisa del tunnel della visione sfocata Dolore alla visione o gonfiore o vedere aloni attorno alle luci;
- Sintomi cardiaci gravi come battiti cardiaci irregolari o martellanti veloci; svolazzando nel petto; fiato corto; e vertigini improvvise Accendino o svenire;
- Grave mal di testa confusione Il braccio del linguaggio bloccato o la debolezza delle gambe problemi perdite perdita di coordinamento sentendoti instabili muscoli molto rigidi ad alta febbre abbondante sudorazione o tremori.
Questo documento non contiene tutti i possibili effetti collaterali e altri possono verificarsi. Verificare con il tuo medico ulteriori informazioni sugli effetti collaterali.
Dosaggio per urso
Il dosaggio degli adulti raccomandato per Urso nel trattamento della PBC è di 13-15 mg/kg/giorno somministrato in due o quattro dosi divise con cibo. Il regime di dosaggio deve essere regolato in base alle esigenze di ciascun paziente a discrezione del medico.
Quali sostanze o integratori di farmaci interagiscono con Urso?
URS può interagire con colestyramina Colestipol estrogeni (pillole anticoncezionali o sostituzione ormonale) o antiacidi che contengono alluminio (come Rolaids Mylanta o Maalox). Dì al tuo medico tutti i farmaci che stai assumendo.
Urso durante la gravidanza o l'allattamento
Durante la gravidanza l'URS dovrebbe essere usato solo quando prescritto. Non è noto se questo farmaco passi nel latte materno. Consulta il medico prima dell'allattamento al seno.
Ulteriori informazioni
Il nostro centro farmacologico URS (Ursodiolo) fornisce una visione completa delle informazioni disponibili sui farmaci sui potenziali effetti collaterali durante l'assunzione di questo farmaco.
Informazioni sui farmaci FDA
- Descrizione del farmaco
- Indicazioni
- Effetti collaterali
- Avvertimenti
- Overdose
- Farmacologia clinica
- Guida ai farmaci
Descrizione per urso
URS 250 (Ursodiolo 250 mg) è disponibile come compressa rivestita di film per la somministrazione orale. Urso Forte (ursodiolo 500 mg) è disponibile come compressa con rivestimento di film punteggi per la somministrazione orale. L'ursodiolo (acido ursodeossicolico UDCA) è un acido bile presente in natura che si trova in piccole quantità nella normale bile umana e in quantità maggiori nelle bile di alcune specie di orsi. È una polvere bianca dal sapore amaro costituito da particelle cristalline liberamente solubili in etanolo e acido acetico glaciale leggermente solubile in cloroformio con parsimonia solubile in etere e praticamente insolubile in acqua. Il nome chimico di ursodiolo è 3α7ß-diidrossi-5ß-Cholan-24-OIC (C24H40O4). Usodiolo ha un peso molecolare di 392,56. La sua struttura è mostrata di seguito.
 |
Ingredienti inattivi: microcristallino cellulosa povidone sodico di sodio glicolato magnesio stearato etilcellulosio dibutil sebacate carnauba idrossipropilcellulosio PEG 3350 peg 8000 alcol -sodio -solfati -solfati e idrogeno.
Usi per urso
Le compresse urso 250 e urso forte (ursodiolo) sono indicate per il trattamento di pazienti con colangite biliare primaria (PBC).
Dosaggio per urso
Informazioni di dosaggio generale
Il dosaggio degli adulti raccomandato per Urso 250 e Urso Forte nel trattamento di PBC è di 1315 mg/kg/giorno somministrato in due o quattro dosi divise con cibo. Il regime di dosaggio deve essere regolato in base alla necessità di ciascun paziente a discrezione del medico.
Test della funzione epatica
I test di funzionalità epatica (γ-GT alcalina fosfatasi AST ALT) e i livelli di bilirubina devono essere monitorati ogni mese per tre mesi dopo l'inizio della terapia e ogni sei mesi in seguito [vedi Avvertimenti e precauzioni ].
Segnare il tablet Urso Forte
Il tablet con punteggio di Urso Forte può essere rotto a metà per fornire dosaggio consigliato.
Per rompere il tablet punteggio di Urso Forte posizionare facilmente il tablet su una superficie piana con la sezione punteggiata in cima. Tenere il tablet con i pollici posizionati vicino alla parte punteggiata del tablet (scanalatura). Quindi applicare una pressione delicata e scattare i segmenti di tablet (i segmenti che si rompono in modo errato non devono essere utilizzati). I segmenti dovrebbero essere lavati in modo non ansito con acqua che mantenendo i segmenti in bocca può rivelare un sapore amaro. A causa dei segmenti di gusto amaro dovrebbero essere conservati separatamente da compresse intere. [Vedere Come fornito / Archiviazione e maneggevolezza ].
Come fornito
Forme di dosaggio e punti di forza
- URSO 250 : Compresse da 250 mg
- Orso stretto : Tablet con punteggio da 500 mg
Archiviazione e maneggevolezza
URSO 250
Ogni compressa ellittica di Biconvex ellittica con rivestimento di pellicola bianca incisa con Urs785 contiene 250 mg di ursodiolo. Disponibile in bottiglie di 100 compresse ( Ndc 58914-785-10).
Orso stretto
Ogni Biconvex ellittico di Urso Forte ha ottenuto una compressa rivestita di film incisa con Urs790 contiene 500 mg di ursodiolo. Disponibile in bottiglie di 100 compresse ( Ndc 58914-79010). Conservare da 20 ° C a 25 ° C (da 68 ° F a 77 ° F). Dispensare in un contenitore stretto.
I medi-tablet (punteggiati di urso forte da 500 mg rotti a metà) mantengono una qualità accettabile per un massimo di 28 giorni se conservati nella confezione corrente (bottiglie) a 20 ° C a 25 ° C (da 68 ° F a 77 ° F). A causa del gusto amaro, i segmenti dimezzati devono essere conservati separatamente dalle compresse intere [vedi Dosaggio e amministrazione ].
Distribuito da: Allergan USA Inc. Madison NJ 07940 www.allergan.com. Revisionato: maggio 2021
Effetti collaterali per urso
Esperienza di studi clinici
Poiché gli studi clinici sono condotti in condizioni di reazione avverse ampiamente variabili osservate negli studi clinici di un farmaco non possono essere confrontati direttamente ai tassi negli studi clinici di un altro farmaco e potrebbero non riflettere i tassi osservati nella pratica clinica.
La tabella seguente riassume le reazioni avverse osservate in due studi clinici controllati con placebo.
| Reazioni avverse | Visita a 12 mesi | Visita a 24 mesi | ||
| UDCA N (%) | Placebo n (%) | UDCA N (%) | Placebo n (%) | |
| Diarrea | --- | --- | 1 (1.32) | --- |
| Creatinina elevata | --- | --- | 1 (1.32) | --- |
| Glicemia elevata | 1 (118) | --- | 1 (1.32) | --- |
| Leucopenia | --- | --- | 2 (2.63) | --- |
| Ulcera peptica | --- | --- | 1 (1.32) | --- |
| Eruzione cutanea | --- | --- | 2 (2.63) | --- |
| Trombocitopeni a | --- | --- | 1 (1.32) | --- |
| Nota: quelle reazioni avverse che si verificano alla stessa o più alta incidenza nel placebo in quanto nel gruppo UDCA sono state eliminate da questa tabella (ciò include diarrea e trombocitopenia a 12 mesi di nausea/vomito e altre tossicità). UDCA = acido ursodeossicolico = ursodiolo |
In uno studio randomizzato incrociato in sessanta pazienti con PBC, sette pazienti (11,6%) hanno riportato nove reazioni avverse: dolore addominale e astenia (1 paziente) nausea (3 pazienti) dispepsia (2 pazienti) e anoressia ed esofagite (1 paziente ciascuno). Un paziente sul regime due volte al giorno (dose totale di 1000 mg) si è ritirato a causa della nausea. Tutte queste nove reazioni avverse tranne l'esofagite sono state osservate con il regime due volte al giorno a una dose giornaliera totale di 1000 mg o superiore. Tuttavia, può verificarsi una reazione avversa in qualsiasi dose.
Esperienza post -marketing
The following adverse reactions presented by system organ class in alphabetical order have been identified during post approval use of ursodiol. Because these reactions are reported voluntarily from a population of uncertain size it is not always possible to reliably estimate their frequency or establish a causal relationship to drug exposure.
- Disturbi gastrointestinali: Disagio addominale Dolore addominale Costipazione Diarrea Dispepsia Nausea Vomito.
- Disturbi generali e condizioni del sito di amministrazione: Malaise Pyrexia edema periferico.
- Disturbi epatobiliari: ittero (o aggravamento di ittero preesistente).
- Disturbi del sistema immunitario: Ipersensibilità al farmaco per includere l'edema facciale orticaria angiedema e l'edema laringeo.
- Test di laboratorio anormali: ALT AST ha aumentato la fosfatasi alcalina nel sangue ha aumentato la bilirubina nel sangue ha aumentato γ-GT aumentato l'enzima epatico aumentato il test di funzionalità epatica aumentata le transaminasi anormali aumentate.
- Disturbi del tessuto muscoloscheletrico e connettivo: mialgia
- Disturbi del sistema nervoso: vertigini mal di testa.
- Disturbi toracici e mediastinali respiratori: tosse.
- Disturbo della pelle e del tessuto sottocutaneo: Alopecia prurito eruzione cutanea.
Interazioni farmacologiche per urso
Agenti sequestri di acido biliare
Anche Gli agenti di sequestro di acidi come la colestiramina e il colestipolo possono interferire con l'azione di Urso 250 e Urso Forte riducendo il suo assorbimento.
Antacidi a base di alluminio
Gli antiacidi a base di alluminio hanno dimostrato di adsorbire acidi biliari in vitro e ci si può aspettare che interferiscano con URS 250 e Urso Forte allo stesso modo degli agenti di sequestro di acidi biliare.
Gli integratori di potassio abbassano la pressione sanguigna
Farmaci che colpiscono il metabolismo lipidico
Gli estrogeni contraccettivi orali e clofibrate (e forse altri farmaci che abbassano i lipidi) aumentano la secrezione epatica del colesterolo e incoraggiano la formazione di calcoli biliari del colesterolo e quindi possono contrastare l'efficacia di URS 250 e Urso Forte.
Avvertimenti per urso
Incluso come parte del PRECAUZIONI sezione.
Precauzioni per urso
I pazienti con ascite di encefalopatia epatica del sanguinamento variceo o che necessitano di un trapianto di fegato urgente devono ricevere un trattamento specifico appropriato.
Test di funzione epatica anormale
I test di funzionalità epatica (γ-GT alcalina fosfatasi AST ALT) e la bilirubina devono essere monitorati ogni mese per tre mesi dopo l'inizio della terapia e ogni sei mesi successivamente. Questo monitoraggio consentirà il rilevamento precoce di un possibile deterioramento della funzione epatica. La discontinuazione del trattamento deve essere considerata se i parametri di cui sopra aumentano a un livello considerato clinicamente significativo nei pazienti con livelli di test epatici storici stabili.
È necessario esercitare cautela per mantenere il flusso biliare dei pazienti che assumono ursodiolo.
Tossicologia non clinica
Mutagenesi della carcinogenesi compromissione della fertilità
In due studi di cancerogenicità orale a 24 mesi nei topi ursodiolo a dosi fino a 1000 mg/kg/giorno (3000 mg/m²/giorno) non era tumorigenico. Sulla base della superficie corporea per una persona di 50 kg di altezza media (1,46 m² di superficie corporea) questa dose rappresenta 5,4 volte la dose clinica massima raccomandata di 15 mg/kg/giorno (555 mg/m²/giorno).
In uno studio di cancerogenicità orale di due anni nel fischer 344 ratti ursodiolo a dosi fino a 300 mg/kg/giorno (1800 mg/m²/giorno 3,2 volte la dose umana massima raccomandata in base alla superficie corporea) non era tumora.
In uno studio di carcinogenicità orale della durata della vita (126-138 settimane) i ratti Sprague-Dawley sono stati trattati con dosi da 33 a 300 mg/kg/giorno da 0,4 a 3,2 volte la dose umana massima raccomandata in base alla superficie del corpo. Usodiolo ha prodotto un significativamente (P<0.5 Fisher's exact test) increased incidence of pheochromocytomas of the adrenal medulla in females of the highest dose group.
Negli studi di carcinogenicità orale di 103 settimane sull'acido litologico un metabolita di dosi di ursodiolo fino a 250 mg/kg/die nei topi e 500 mg/kg/die nei ratti non ha prodotto tumori. In uno studio di ratto di 78 settimane Instillazione intarettale di acido litologico (1 mg/kg/giorno) per 13 mesi non ha prodotto tumori del colon-retto. È stato osservato un effetto che promuove il tumore quando è stato somministrato dopo una singola dose intraarettale di un noto cancerogeno N-metil-N'-nitro-N-nitrosoguanidina. D'altra parte in uno studio di ratto di 32 settimane ursodiolo alla dose giornaliera di 240 mg/kg (1440 mg/m² 2,6 volte la dose umana massima raccomandata basata sulla superficie corporea) ha soppresso l'effetto carcinogeno del colon di un altro azoxymetane cancerogeno noto.
L'ursodiolo non era genotossico nel test Ames della cellula del linfoma del topo (L5178Y TK /-) Test di mutazione in avanti Il test di scambio cromatidico della sorella linfocita umana il test dell'aberrazione del cromosoma del cromosoma cinese e il test dell'aberrazione del cromosoma del cromosoma cinese.
Usodiolo a dosi orali fino a 2700 mg/kg/die (16200 mg/m²/giorno 29 volte la dose umana massima raccomandata in base alla superficie corporea) è stato scoperto che non ha alcun effetto sulla fertilità e sulle prestazioni riproduttive dei ratti maschi e femmine.
Utilizzare in popolazioni specifiche
Gravidanza
Riepilogo del rischio
Disponibili dati pubblicati sull'uso di ursodiolo nelle donne in gravidanza derivate da studi di osservazione controllati randomizzati e serie di casi raccolte nel corso di diversi decenni non hanno identificato un rischio associato al farmaco di gravi aborti di difetti alla nascita o altri esiti avversi materni o fetali. La maggior parte delle esposizioni riportate a ursodiolo si sono verificate nel secondo e terzo trimestre di gravidanza. Negli studi sulla riproduzione degli animali l'ursodiolo non ha avuto effetti avversi sullo sviluppo embrionale quando somministrato a dosi maggiori delle dosi terapeutiche umane (vedi Dati ).
Il rischio di background stimato di principali difetti alla nascita e aborto spontaneo per la popolazione indicata non è noto. Tutte le gravidanze hanno un rischio di fondo di perdita di difetti alla nascita o altri risultati avversi. Nella popolazione generale degli Stati Uniti il rischio di background stimato di gravi difetti alla nascita e aborto spontaneo nelle gravidanze clinicamente riconosciute è rispettivamente dal 2 al 4% e dal 15 al 20%.
Dati
Dati sugli animali
Non sono stati osservati effetti avversi sullo sviluppo dell'embrione-fetale con la somministrazione orale di ursodiolo a ratti e conigli in gravidanza durante l'organogenesi a dosi fino a 22 e 7 volte rispettivamente la massima dose umana raccomandata (basata sulla superficie corporea).
pillole 101
Lattazione
Riepilogo del rischio
Usodiolo è naturalmente presente nel latte umano. Non ci sono segnalazioni di effetti avversi di ursodiolo sul bambino allattato al seno, ma i rapporti sono estremamente limitati. Non ci sono dati sugli effetti dell'ursodiolo sulla produzione di latte. I benefici per lo sviluppo e la salute dell'allattamento dovrebbero essere considerati insieme alla necessità clinica della madre per URS 250 e Urso Forte e qualsiasi potenziale effetto avverso sul bambino allattato al seno da Urso 250 e Urso Forte o dalla condizione materna sottostante.
Uso pediatrico
La sicurezza e l'efficacia di Urso 250 e Urso Forte nei pazienti pediatrici non sono stati stabiliti.
Informazioni per overdose per urso
Non ci sono state segnalazioni di sovradosaggio accidentale o intenzionale con ursodiolo. Le singole dosi orali di ursodiolo a 10 g/kg in topi e cani e 5 g/kg nei ratti non erano letali. Una singola dose orale di ursodiolo a 1,5 g/kg era letale nei criceti. I sintomi della tossicità acuta sono stati la salivazione e il vomito nei cani e con le convulsioni agonali della dispnea di dispnea di atassia e coma nei criceti.
Controindicazioni per orso
Pazienti con ostruzione biliare completa e ipersensibilità nota o intolleranza all'ursodiolo o a uno qualsiasi dei componenti della formulazione.
Farmacologia clinica for Urso
Meccanismo d'azione
Ursodiolo Un acido bile idrofilo naturale derivato dal colesterolo è presente come una frazione minore del pool di acido bile umano totale. La somministrazione orale di ursodiolo aumenta questa frazione in modo dose per diventare il principale acido biliare che sostituisce/sposta le concentrazioni tossiche di acidi biliari idrofobici endogeni che tendono ad accumularsi nella malattia epatica colestatica. Oltre alla sostituzione e allo spostamento degli acidi biliare tossici, altri meccanismi d'azione includono la citoprotezione delle cellule epiteliali del dotto biliare ferito (colangiociti) contro gli effetti tossici degli acidi bile dell'inibizione degli epatociti degli epatociti e degli effetti immunovini immunovisti.
Farmacodinamica
L'acido litocholico quando somministrato cronicamente agli animali provoca lesioni epatiche colestatiche che possono portare alla morte per insufficienza epatica in alcune specie incapaci di formare coniugati di solfato. L'ursodiolo è 7-detidrossilato più lentamente del chenodiol. Per le dosi equimolari di ursodiolo e chenodiol, livelli di acido litocholico sono più bassi durante la somministrazione di ursodiolo rispetto alla somministrazione di chenodiol. Gli esseri umani e gli scimpanzé possono solfare l'acido litocholico. Sebbene la lesione epatica non sia stata associata alla terapia con ursodiolo, in alcuni individui può esistere una ridotta capacità di solfato.
Farmacocinetica
Ursodiolo (UDCA) è normalmente presente come una frazione minore degli acidi biliari totali nell'uomo (circa il 5%). Dopo la somministrazione orale la maggior parte dell'ursodiolo viene assorbita dalla diffusione passiva e il suo assorbimento è incompleto. Una volta assorbito l'ursodiolo subisce un'estrazione epatica nell'entità di circa il 50% in assenza di malattie epatiche. Man mano che la gravità della malattia epatica aumenta l'entità dell'estrazione diminuisce. Nel fegato l'ursodiolo è coniugato con glicina o taurina, quindi secreto in bile. Questi coniugati di ursodiolo sono assorbiti nell'intestino tenue da meccanismi passivi e attivi. I coniugati possono anche essere deconjugati nell'ileo dagli enzimi intestinali che portano alla formazione di ursodiolo libero che può essere riassorbito e riconjugati nel fegato. L'ursodiolo non assorbito passa nel colon dove è per lo più 7-deidrorossilato in acido litocholico. Alcuni ursodiol vengono epimerizzati in chenodiol (CDCA) tramite un intermedio 7-oxo. Chenodiolo subisce anche 7-deidrossilazione per formare l'acido litocholico. Questi metaboliti sono scarsamente solubili ed escreti nelle feci. Una piccola porzione di acido litocholico viene riassorbita coniugato nel fegato con glicina o taurina e solfatata nella posizione 3. I coniugati di acido litologico solfato risultante vengono escreti in biliare e quindi persi nelle feci.
In soggetti sani almeno il 70% di ursodiolo (non coniugati) è legato alla proteina plasmatica. Non sono disponibili informazioni sul legame di ursodiolo coniugato con la proteina plasmatica in soggetti sani o pazienti con PBC. Il suo volume di distribuzione non è stato determinato ma dovrebbe essere piccolo poiché il farmaco è per lo più distribuito nella bile e nell'intestino tenue. L'ursodiolo viene escreto principalmente nelle feci. Con il trattamento gli aumenti dell'escrezione urinaria ma rimane meno dell'1% tranne nella grave malattia epatica colestatica.
Durante la somministrazione cronica di ursodiolo diventa un grande acido biliare biliare e plasma. Ad una dose cronica da 13 a 15 mg/kg/giorno, l'ursodiolo costituisce il 30-50% di acidi biliare biliare e plasmatica.
Studi clinici
Efficacia dell'acido ursodeossicolico somministrato a 13-15 mg/kg/giorno in 3 o 4 dosi divise a pazienti con PBC
È stato condotto uno studio randomizzato in doppio cieco randomizzato negli Stati Uniti per valutare l'efficacia dell'acido ursooxicvolico alla dose da 13 a 15 mg/kg/giorno somministrato in 3 o 4 dosi divise in 180 pazienti con PBC (78% ha ricevuto quattro volte al giorno dosaggio). Al completamento della porzione in doppio cieco, tutti i pazienti sono entrati in una fase di estensione del trattamento attivo in aperto.
Incapacità del trattamento Il principale endpoint di efficacia misurato durante questo studio è stato definito come necessità di morte per il trapianto di trapianto di fegato di progressione istologica da parte di due stadi o per lo sviluppo della cirrosi di varici ascite o encefalopatia marcata il peggioramento della fatica o dell'incapacità della prurito di tollerare il farmaco raddoppiando il drogato di bilirubina e ritiro volontario. Dopo due anni di trattamento in doppio cieco, l'incidenza del fallimento del trattamento era significativamente (p<0.01) reduced in the URSO 250 mg group (20 of 86 (23%) as compared to the placebo group (40 of 86 (47%). Time to treatment failure which excluded doubling of serum bilirubin and voluntary withdrawal was also significantly (p<0.001) delayed in the URSO 250 treated group (n=86 803.8±24.9 d vs. 641.1±24.4 d for the placebo group (n=86) on average) regardless of either histologic stage or baseline bilirubin levels (>1.8 o <1.8 mg/dL).
L'uso di una definizione di fallimento del trattamento che ha escluso il raddoppio della bilirubina sierica e il tempo di ritiro volontario per il fallimento del trattamento è stato significativamente ritardato nel gruppo URS 250. In confronto al trattamento con placebo con URS 250 ha comportato un miglioramento significativo nei seguenti biochimistrie epatiche sieriche rispetto al basale: fosfatasi alcalina SGOT di bilirubina totale e IgM.
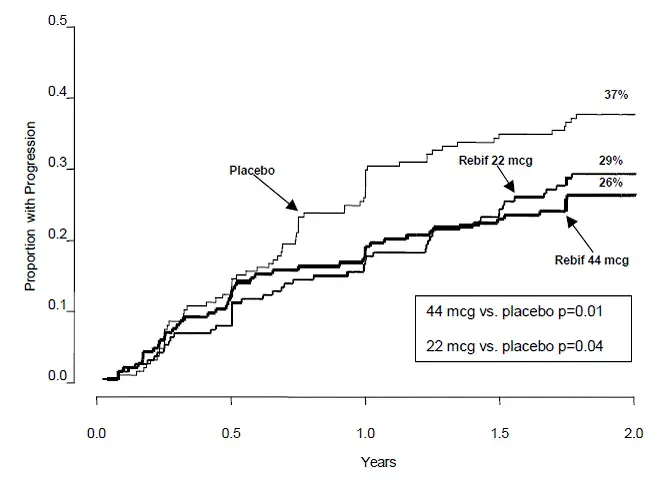
Efficacia di ursodiolo somministrato a 14 mg/kg/giorno come dose una volta giornaliera ai pazienti con PBC
Un secondo studio condotto in Canada randomizzato 222 pazienti PBC a ursodiolo 14 mg/kg/giorno o placebo somministrato come dose una volta giornaliera in modo in doppio cieco durante un periodo di due anni. A due anni un statisticamente significativo (P<0.001) difference between the two treatments (n=106 for the URSO 250 group and n=106 for the placebo group) in favor of ursodiol was demonstrated in the following: reduction in the proportion of patients exhibiting a more than 50% increase in serum bilirubin; median percent decrease in bilirubin (-17.12% for the URSO 250 group vs. +20.00% for the placebo group) transaminases (-40.54% for the URSO 250 group vs. +5.71% for the placebo group) and alkaline phosphatase (-47.61% for the URSO 250 group vs. -5.69% for the placebo group); incidence of treatment failure; and time to treatment failure. The definition of treatment failure included: discontinuing the study for any reason; a total serum bilirubin level greater than or equal to 1.5 mg/dl or increasing to a level equal to or greater than two times the baseline level; and the development of ascites or encephalopathy. Evaluation of patients at 4 years or longer was inadequate due to the high drop-out rate (n=10 withdrew from the URSO 250 group vs. n=15 from the placebo group) and small number of patients. Therefore death need for liver transplantation histological progression by two stages or to cirrhosis development of varices ascites or encephalopathy marked worsening of fatigue or pruritus inability to tolerate the drug doubling of serum bilirubin and voluntary withdrawal were not assessed.
Efficacia di URS 250 somministrata in due volte al giorno rispetto a quattro volte al giorno Assegni di dosaggio diviso per i pazienti con PBC
Uno studio di crossover a due periodi randomizzato in cinquanta pazienti con PBC ha confrontato l'efficacia di URS 250 (ursodiolo) in programmi di dosaggio di due volte al giorno contro quattro volte al giorno in 50 pazienti per 6 mesi in ciascun periodo di crossover. Le variazioni percentuali medie rispetto al basale nei risultati dei test epatici e il punteggio del rischio di Mayo (n = 46) e l'arricchimento sierico con UDCA (n = 34) non erano statisticamente significative con alcun dosaggio a qualsiasi intervallo di tempo. Questo studio ha dimostrato che l'UDCA (da 13 a 15 mg/kg/giorno) dato due volte al giorno è ugualmente efficace per l'UDCA somministrato quattro volte al giorno. Inoltre, URS 250 è stato somministrato come un singolo rispetto a tre volte al giorno gli orari di dosaggio in 10 pazienti. A causa del piccolo numero di pazienti in questo braccio dello studio, non era possibile condurre confronti statistici tra questi regimi.
Informazioni sul paziente per urso
Trattamenti appropriati
I pazienti con le seguenti condizioni devono essere istruiti a ricevere misure di gestione appropriate: ascite di encefalopatia epatica del sanguinamento variceo che necessita di un trapianto di fegato urgente o di una funzione epatica di deterioramento [vedi Avvertimenti e precauzioni ].
È necessario esercitare cautela per mantenere il flusso biliare dei pazienti che assumono ursodiolo.
Interazioni farmacologiche
I pazienti devono essere informati che l'assorbimento di URS 250 e Urso Forte può essere ridotto se stanno assumendo agenti sequestri di acido biliare come antiacidi o farmaci a base di colestiro Interazioni farmacologiche ].